Einleitung
Es handelt sich um einen Zucht- und Mastbetrieb mit 350 Sauen in Nordirland.

Der Betrieb war negativ auf Enzootische Pneumonie (Mycoplasma hyodysenteriae), Porzine Pleuropneumonie (Actinobacillus pleuropneumoniae), Schweineinfluenza und PRRS (Porzines Reproduktives und Respiratorisches Syndrom).
Tabelle 1 zeigt den verwendeten Impfplan.
Tabelle 1: Impfplan.
| Impfstoff | Jungsauen | Sauen | Eber | Ferkel |
|---|---|---|---|---|
|
Parvovirus + Erysipel + Leptospirose |
Injektion von 2 ml bei der Auswahl der Tiere und 2 Wochen vor der Deckung | Injektion von 2 ml 2 Wochen vor der Deckung | Injektion von 2 ml zweimal pro Jahr | |
| Eigenimpfstoff (Streptococcus suis & Staphylococcus hyicus) | 2 ml am Tag 65 nach der Deckung und am Tag 95 nach der Deckung | 2 ml am Tag 95 nach der Deckung |
Die Jungsauen wurden im Betrieb selbst gezüchtet. Eber dienten der Stimulierung. Jungsauen und Sauen wurden mit Samen aus einem einzigen Zuchtbetrieb künstlich besamt.
Der nächste Schweinebetrieb war 6 km entfernt.
Krankengeschichte
Der Landwirt kontaktierte den Tierarzt aufgrund zunehmender Atemnot und Mortalität bei Mastschweinen in den vergangenen 3 Tagen.
Untersuchung
3.1 Klinische Untersuchung
Bei einem Besuch des Betriebs im November 2017 gab es viele 18 bis 24 Wochen alte Ferkel mit klinischen Symptomen von Husten (Abb. 1 & Videos 1 & 2) und Zyanose der unteren und distalen Körperteile. Der Futtertrog für Flüssigfutter war nicht leer, was auf Appetitlosigkeit hindeutete. Von einigen klinisch betroffenen Tieren, die Fieber hatten, wurden die Rektaltemperaturen gemessen. Der Körperzustand der Tiere war normal.

Abbildung 1: Schwein mit Husten in einem Krankenstall. Hinweis: Der Futterautomat im Krankenstall gibt Trockenfutter ad libitum aus.
Video 1: Klinisch erkrankte Schweine mit Husten
2 Wochen später wurde der Betrieb ein zweites Mal besucht, um von den Zuchttieren und den Mast-/Endmastschweinen Blutproben zu entnehmen.
Die Mortalität vom Absetzen bis zur Mast betrug vor dem Ausbruch der Krankheit 3,5 %, was meist mit Tieren in Verbindung stand, die als Folge einer Herniation und/oder eines Rektumprolapses eingeschläfert werden mussten.
3.2. Laboruntersuchungen
Im November 2017 wurden drei Tote Schweine im Betrieb seziert (Abb. 2).
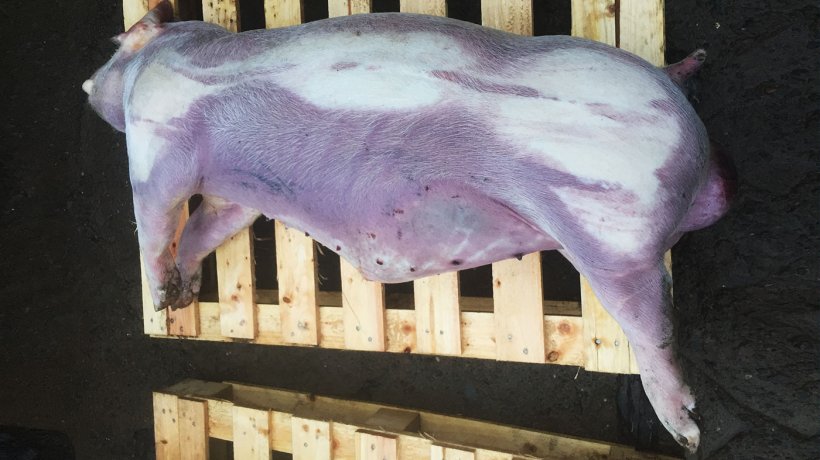
Abbildung 2: Mastschwein mit Zyanose der unteren und distalen Körperteile
Bei allen 3 sezierten Schweinen gab es multiple Petechien im Lungenparenchym (Abb. 3). Die entnommenen Proben wurden dem Labor zur Analyse übergeben.
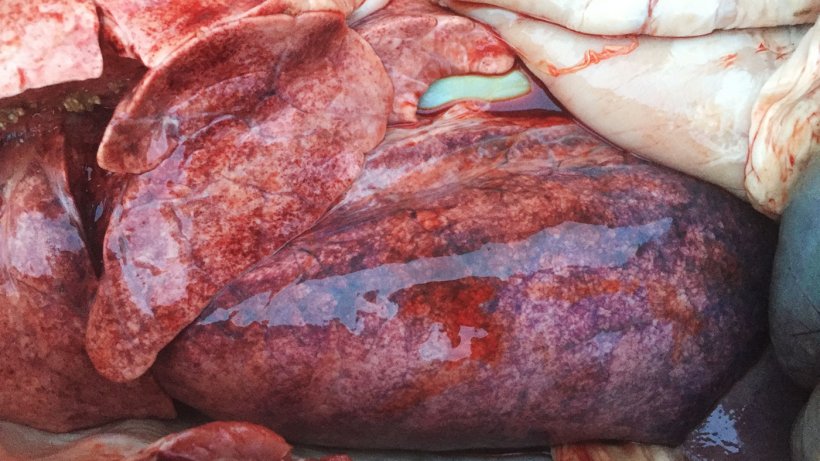
Abbildung 3: Multiple Petechien im Lungenparenchym
Die Laboruntersuchungen der Lungen sind in Tabelle 2 zusammengefasst.
Tabelle 2: Laborergebnisse von drei eingereichten Lungen
| Bakteriologischer Befund | Biomolekularer Befund | |
|---|---|---|
| Lunge 1 | Kein Wachstum | Negativ auf Mycoplasma hyopneumoniae & PRRS durch RT-PCR. Positiv auf Influenzavirus Typ A durch RT-PCR (Ct-Wert: 18,1) Subtyp H1N1 |
| Lunge 2 | Kein Wachstum | Negativ auf Mycoplasma hyopneumoniae & PRRS durch RT-PCR. Positiv auf Influenzavirus Typ A durch RT-PCR (Ct-Wert: 26,9) Subtyp H1N1 |
| Lunge 3 | Kein Wachstum | Negativ auf Mycoplasma hyopneumoniae & PRRS durch RT-PCR. Positiv auf Influenzavirus Typ A durch RT-PCR (Ct-Wert: 31,5) Subtyp H1N1 |
Die histologische Untersuchung des Lungengewebes zeigte eine lymphozytische Infiltration der Lamina propia und der Tela submucosa der Bronchien (Abb. 4 & 5).
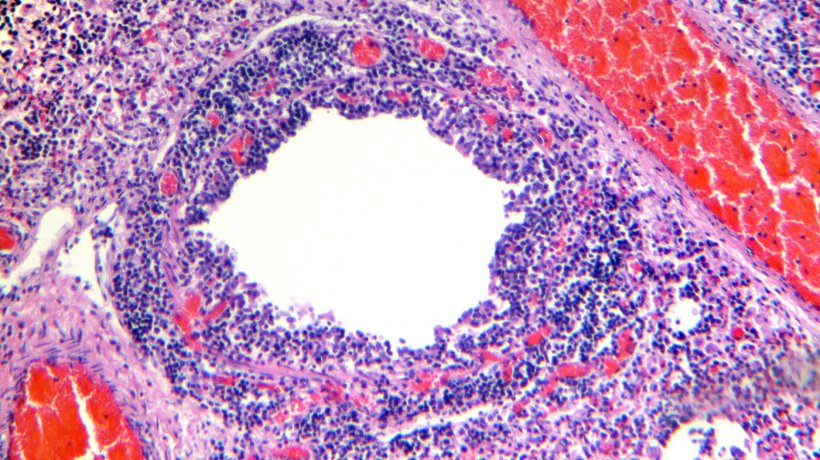
Abbildung 4: Bronchiole, die Desquamation und Nekrose des Atemwegsepithels, zusammen mit einer ausgeprägten lymphozytischen Infiltration der Lamina propia und der Tela submucosa aufweist.
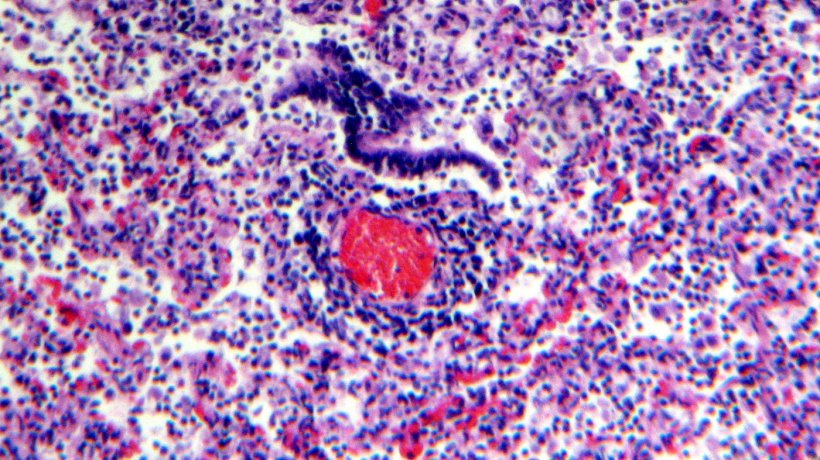
Abbildung 5: Perivaskuläre Lymphozyteninfiltration
Die Laboruntersuchungen der 14 Blutproben, die von dem Zucht- und Mastbetrieb entnommen wurden, sind in Tabelle 3 zusammengefasst.
Tabelle 3: Laborergebnisse von den 14 entnommenen Blutproben
| PRRS (ELISA) | Influenza A (ELISA) | Actinobacillus pleuropneumoniae (ELISA) | PCV-2 (ELISA) | Mycoplasma hyopneumoniae (ELISA) | |
|---|---|---|---|---|---|
| 3 x 12 Wochen alte Schweine mit Schnupfen | 3 (-) | 2 (+) 1 (-) |
3 (-) | 3 (-) | 3 (-) |
| 2 x genesene Schweinen | 2 (-) | 1 (+) 1 (-) |
2 (-) | 2 (-) | 2 (-) |
| 2 x Ferkel von verschiedenen Sauen mit Husten | 2 (-) | 2 (+) | 2 (-) | 2 (-) | 2 (-) |
| 7 x Sauen | 7 (-) | 7 (+) | 7 (-) | 7 (-) | 7 (-) |
Die positiven Influenza-A-Proben wurden auf Antikörper gegen die Subtypen H1N1, H3N2 & H1N2 und die Pandemie-Subtypen panH1N1 und panH1N2 getestet. Bei den erkrankten Tieren wurden sehr hohe Antikörpertiter (≥ 320 bis 2560) gegen all diese Subtypen nachgewiesen, was auf eine kürzliche Infektion hindeutet.
4. Differentialdiagnose
Auf Grundlage der klinischen Untersuchungen und der Labortests wurde die folgende Liste der Differentialdiagnosen erstellt:
- PRRS (Porzines Reproduktives und Respiratorisches Syndrom)
- Influenzavirus Typ A (Grippe)
- Enzootische Pneumonie (Mycoplasma hyopneumoniae)
- Porzine Pleuropneumonie (Actinobacillus pleuropneumoniae)
Aufgrund der Krankengeschichte und der einheitlichen Ergebnisse der klinischen Untersuchungen und der Labortests wurde die Diagnose einer akuten Infektion mit dem Influenzavirus Typ A gestellt.
5. Programm zur Bekämpfung
In diesem Betrieb wurde das folgende Notfallprogramm zur Bekämpfung der Grippe durchgeführt:
- Eine zweimalige Massenimpfung aller Zuchtbestände im Abstand von 3 Wochen zwischen den jeweiligen Injektionen.
- Schweine wurden beim Absetzen mit 2 ml eines kommerziellen Grippeimpfstoffs geimpft, sobald man die Virusinfektion diagnostiziert hatte.
- Das Futter aller Schweine wurde 20 Tage lang mit 85 ppm Tylvalosintartrat pro Tonne versetzt, um Erregern von Atemwegserkrankungen entgegenzuwirken.
Nachdem der gesamte Zuchtbestand zweimal gegen Grippe immunisiert worden war, wurden die folgenden Maßnahmen ergriffen:
- Eine zweimalige Impfung der Jungsauen vor der Deckung im Abstand von 3 Wochen zwischen den beiden Injektionen.
- Der Zuchtbestand erhielt 14 Tage vor dem Abferkeln eine Auffrischungsimpfung mit einer Dosis.
Leider deckten die gängigen Grippeimpfstoffe, die zum Zeitpunkt des Ausbruchs im Land erhältlich waren, die pandemischen Subtypen panH1N1 und panH1N2 nicht ab. Seit September 2018 wird im Zuchtbetrieb ein Grippeimpfstoff als Vorsichtsmaßnahme verabreicht, der die pandemischen Subtypen abdeckt.
6. Reaktion auf das Programm zur Bekämpfung
Es gab einen Anstieg der Sterblichkeit von 3,5 % zu Beginn des Ausbruchs auf 11,5 % an dessen Höhepunkt 4 Wochen später. 10 Wochen nach Beginn des Ausbruchs verringerte sich die Sterblichkeit allmählich auf das normale Niveau.
Die Trächtigkeitsrate sank zwei Monate lang von 94 % auf 86 %. Dies spiegelte sich in einer Reduktion der Abferkelrate von 91 % auf 84 % im gleichen Zeitraum wider. Es gab keine Aborte.
7. Diskussion
Die Schweinegrippe ist eine akute, infektiöse Atemwegserkrankung von Schweinen, die durch Influenza-Viren des Typs A verursacht wird. Die Krankheit ist vom plötzlichem Auftreten von Husten, Atemnot, Fieber und Erschöpfung geprägt, worauf eine rasche Genesung folgt. Die Läsionen entwickeln sich in der Regel sehr rasch in den Atemwegen und gehen schnell wieder zurück, aber in einigen Fällen kann eine schwere virale Pneumonie folgen, die zum Tod führt (Ostertag et al., 1999). Bei der klinischen Untersuchung dieses Falles wurden all diese klinischen Symptome festgestellt.
Die Schweinegrippe wird durch Influenza-A-Viren der Familie Orthomyxoviridae verursacht. Es gibt Unmengen an Informationen über die antigenischen, genetischen, strukturellen und biologischen Eigenschaften von Influenza-A-Viren (Murphy et al., 1990; Lamb et al., 1996). Die beiden Oberflächenglykoproteine des Virus Hämagglutinin (H) und Neuraminidase (N) sind die wichtigsten Antigene, die die schützende Immunität im Wirt verleihen, und zeigen daher die größten Variationen.
Die Überwachung, die von 2011 bis 2013 in Nordirland durchgeführt wurde, zeigte, dass der pandemische H1N1-Stamm der wichtigste Subtyp ist, der bei Schweinen isoliert wurde, gefolgt von den anderen Subtypen (H1N1, H3N2) mit geringerem Auftreten (Borobia et al., 2015).
Die Witterungsbedingungen begünstigten zum Zeitpunkt dieses Ausbruchs die Ausbreitung des Virus. Es war die letzten 3 Monate feucht mit schwankenden Temperaturen und starken Winden dazwischen. Es ist wahrscheinlich, dass Menschen oder Stare (Abb. 6) einige Schweine durch den engen Kontakt oder durch die Nähe zu anderen Schweinebetrieben durch aerogene Übertragung infiziert haben. Im vorliegenden klinischen Fall dürften tatsächlich beide Möglichkeiten aufgetreten sein.

Abbildung 6: Stare in direktem Kontakt mit Endmastschweinen, die die Futterreste im Schweinetrog fressen.
Wie auch hier zu sehen ist, wird die Sterblichkeit bei Schweinegrippe als hoch bezeichnet (fast 100 %) (Taylor, 1995; Ostertag et al., 1999). Taylor (1995) und Easterday et al. (1999) berichten von einer Sterblichkeitsrate von weniger als 1 %, es sei denn, es gibt interkurrente Infektionen und/oder die Schweine sind sehr jung.
Leider lag, wie bereits erwähnt, die Sterblichkeit in diesem Fall über 1 %.
Probleme bei der Fortpflanzung, der Geburt und bei den neugeborenen Ferkeln wurden in Zusammenhang mit der Schweinegrippe in der Literatur von verschiedenen Autoren beschrieben (Taylor, 1995; Muirhead et al., 1997; Ostertag et al., 1999; Jackson et al., 2007). In unserem Fall zeigten sie sich allerdings nur in der schlechten Trächtigkeits- und Abferkelrate.
Das Versetzen des Futters mit Tylvalosintartrat erfolgte auf Grundlage von Befunden von Dr. David Brown und Dr. Amanda Stuart aus der Pathologieabteilung der Universität Cambridge. Die Wirkung dieses Makrolidantibiotikums auf PRRS reduzierte im Gegensatz zu Tylosin, einem anderen Makrolidantibiotikum, die Anzahl der in vitro infizierten Zellen. Tylvalosin reduzierte auch die Anzahl der Zellen, die von mehreren anderen Viren infiziert wurden, darunter menschliche Influenza- und Pferdeinfluenza-Viren (Brown et al., 2006).
Darüber hinaus verfügt Tylvalosin über eine bessere intrazelluläre Akkumulation und Verteilung zur Behandlung klinischer Krankheiten als andere Makrolide (Stuart et al., 2007).






