Dieser Fall einer Blastocystis-Infektion in Absetzferkeln wurde im März 2015 in einem Ferkelproduktionsbetrieb beobachtet. In diesem geschlossenen und kombinierten Betrieb werden Ferkel mit 60 Zuchtsauen in einem 3-Wochen-Rhythmus mit einer Säugezeit von 28 Tagen produziert. Sauen werden routinemäßig gegen Parvovirose und Rotlauf geimpft und Ferkel gegen PCV-2 und Mycoplasma hyopneumoniae. Bezüglich anderer Schweinekrankheiten gab es keine Informationen.

Symptome
Der betreuende Tierarzt berichtete, dass Durchfall bei Ferkel nach dem Absetzen auftritt. Mehrere Therapiemaßnahmen, wie z.B. Antibiose und Anpassung des Futters, führten zu keinem Erfolg. Die Die Mortalitätsrate betrug 5%. Die einzigen klinischen Symptome, die auffielen, waren verminderte Gewichtszunahme und Durchfall. Zu diesem Zeitpunkt wurden wir von der Universitätsklinik für Schweine konsultiert und um Hilfestellung in diesem Fall gebeten.
Klinische Untersuchung und eingeleitete diagnostische Maßnahmen
An die Universitätsklinik für Schweine wurde ein Ferkel gebracht, welches aber mit Colistin (5mg/kg Körpergewicht/Tag für 7 Tage) vorbehandelt wurde. Dieses Tier zeigte typischen profusen Durchfall. Bei der klinischen Untersuchung konnte nur ein mittelgradig verminderter Ernährungszustand und Durchfall festgestellt werden. Nach der klinischen Untersuchung wurde das Ferkel euthanasiert, um eine Sektion und pathohistologische Untersuchung durchführen zu können. Ein Stück Jejunum wurde für die bakteriologische Untersuchung entnommen. Für den kulturellen Nachweis von Brachyspiren wurde ein Gefäß randvoll mit Durchfallkot befüllt (Herstellung anaerober Bedingungen), und sofort an das Institut für Bakteriologie übermittelt. Eine PCV-2 in-situ Hybridisierung in formalin-fixiertem Darmgewebe wurde angefertigt, um eine Beteiligung von PCV-2 auszuschließen. Des Weiteren wurde ein Darmgeschabsel (Ileum- und Kolonschleimhaut) auf die Anwesenheit von Lawsonia intracellularis, Brachyspira hyodysenteriae und Brachyspira pilosicoli mittels Triplex-PCR untersucht. Zum Nachweis von Kokzidienoozysten oder anderen Protozoen wurde eine fluoreszenzmikroskopische und lichtmikroskopische Untersuchung von Kot durchgeführt.
Pathologische Befunde
In den Organen konnten keine nennenswerten pathomorphologischen Veränderungen festgestellt werden. Der Darminhalt im Kolon war hellgrün und flüssig. In der Mukosa des Dünndarms waren auffallend viele eosinophile Granulozyten zu finden. Sowohl die PCV-2 in-situ Hybridisierung als auch die Triplex-PCR erbrachten ein negatives Ergebnis.
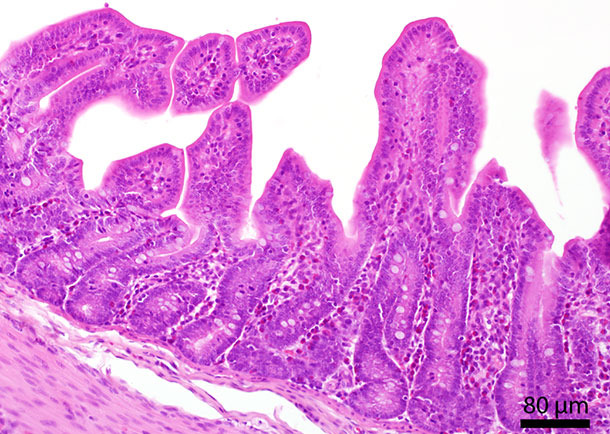
Abb. 1: Histologischer Schnitt eines Dünndarms. In der Mukosa sind zahlreiche eosinophile Granulozyten zu sehen.
Bakteriologische Befunde
Im Jejunum konnten nur vereinzelt hefeähnliche Pilze und vereinzelt Escherichia coli nachgewiesen werden. Aufgrund des geringgradigen Nachweisgrades von E. coli im Jejunum wurde die klinische Relevanz dieses Stammes als gering eingestuft und deshalb keine Virulenzfaktorbestimmung durchgeführt. Kulturell konnten keine Brachyspira spp. nachgewiesen werden.
Parasitologische Befunde
Fluoreszenzmikroskopisch konnten keine Kokzidienoozysten gefunden werden. Neobalantidium coli-Zysten wurden in einem Ausmaß nachgewiesen, welche physiologischer Weise im Dickdarm von gesunden Tieren in diesem Ausmaß vorkommen.
Bei der lichtmikroskopischen Untersuchung konnten massenhaft rundliche Strukturen in der Größe von 10-20 µm im Kot beobachtet werden. Diese Objekte erschienen als transparent mit keinem oder fast keinem „intrazellulären“ Inhalt (Abb. 1).
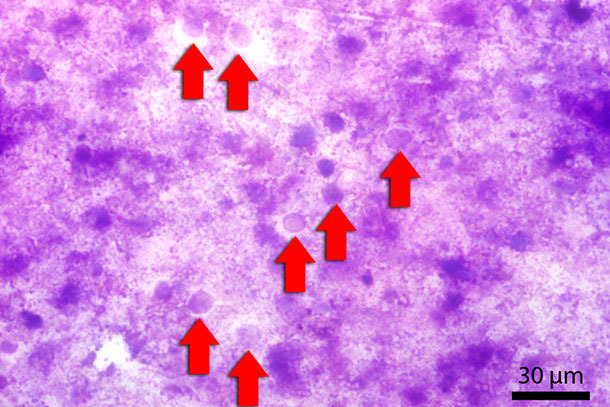
Abb. 2: Kotausstrich mit Diff-Quick gefärbt. Die roten Pfeile zeigen auf Blastocystis-Stadien.
Um diese Objekte näher zu untersuchen wurde ein Kotausstrich angefertigt und mittels Diff-Quick Färbekit gefärbt. Bei einer 1000-fachen Vergrößerung unter Verwendung von Immersionsöl konnten diese Objekte als einzellig und hauptsächlich basophil wiedergefunden werden. Da nach unserem Wissen diese Strukturen normalerweise nicht in diesem Ausmaß in Schweinekot gefunden werden, wurde angenommen es handle sich hierbei um etwas „Neues“. Nach Konsultation von Pathologen, Bakteriologen und Parasitologen, kam die finale Diagnose von einem Protistologen, der mit veterinärmedizinisch und humanmedizinisch relevanten Einzellern arbeitet. Er konnte diese rundlichen Objekte eindeutig als Blastocystis sp. bestimmen.
Interpretation der Befunde
Da in diesem Fall kein bekanntes Enteropathogen in klinisch relevanten Mengen nachgewiesen werden konnte, wurde die Bedeutung von Blastocystis sp. als wesentlich eingestuft.
Blastocystis sp. ist ein Einzeller, welcher immer wieder im Menschen und in Tieren, wie zum Beispiel in Schweinen und Rindern nachgewiesen werden kann. Die Zelle ist von einer Zellmembran umgeben, welche zentral eine große Vakuole enthält. Der Zellkern liegt dicht am Rand (Abb. 2). Erstmals wurde dieser Einzeller 1911 beschrieben, wobei Pathogenese und Pathogenität nach wie vor nicht zur Gänze bekannt ist. Im Schwein kommt Blastocystis sp. physiologisch in mäßigen Mengen im Dickdarm vor. In Studien in welchen Blastocystis-Infektionen in immunsupprimierten Schweinen untersucht wurden, konnte eine höhere Wahrscheinlichkeit für den Nachweis von Blastocystis im Kolon aber genauso im Dünndarm gefunden werden. Läsionen und Kolonisierung des Epithels konnten weder beim Menschen noch beim Schwein festgestellt werden.
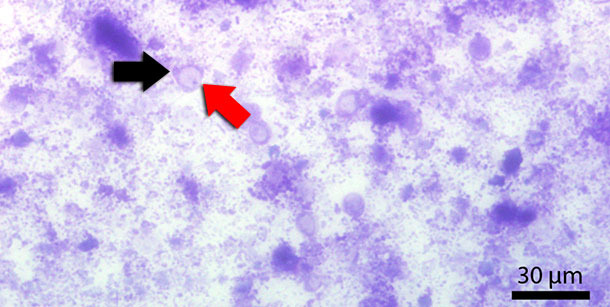
Abb. 3: Kotausstrich mit Diff-Quick gefärbt. Der rote Pfeil zeigt auf die zentrale Vakuole. Der schwarze Pfeil zeigt auf den Zellkern.
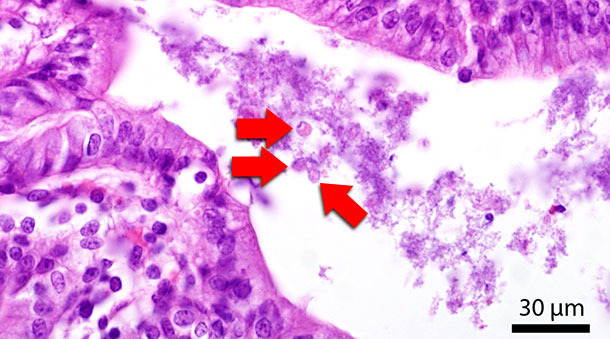
Abb. 4: Histologischer Schnitt des Dickdarms. Die roten Pfeile zeigen auf Blastocystis-Stadien im Darmlumen.
Im aktuellen Fall wurde vermutet, dass eine Belastung mit Mykotoxinen zur massiven Kolonisierung des Ferkeldarmes führte. Im Jahr 2014 gab es eine außergewöhnliche Mykotoxinbelastung in Mitteleuropa vor allem von Mais, im Speziellen mit Toxinen aus der Gruppe der A und B Trichothecene. Deoxynivalenol (DON), zur Gruppe der B Trichothecene gehörend und T2-Toxin zur Gruppe der A Trichothecene gehörend sind Mykotoxine, welche für ihre immunsuppressive Wirkung bekannt sind. Aufgrund der generell hohen Mykotoxinbelastung des Mais der letzten Ernte wurde auf diesem Betrieb entschieden, den Mais aus der Ration zu entfernen. Nichtsdestotrotz sind Mykotoxine mit großer Wahrscheinlichkeit (vorwiegend T2 und DON) die initialen immunsuppressiven Komponenten, welche eine Kolonisierung des Darms mit Blastocystis sp. von Ferkeln vorangegangener Partien steigerten und unterstützten. Das in Kombination mit einer fehlenden Desinfektion könnte zu einer außergewöhnlichen Kontamination der Buchten mit infektiösen Blastocystis-Stadien geführt haben, welche nachfolgende Partien belastete.
Prophylaxe und Therapie
Die Behandlung der Blastocystose ist schwierig, da nur eine begrenzte Anzahl an wirksamen Substanzen zur Verfügung steht. Mittel der Wahl für eine antibiotische Behandlung wäre Metronidazol, welches aber in der gesamten EU für lebensmittelliefernde Tiere weder registriert noch zugelassen ist. Auch andere gut wirksame Imidazole wie Tinidazol und Ketokonazol sind weder registriert noch zugelassen.
Im Moment besteht die Möglichkeit Blastocystose mit Trimethoprim-Sulfonamid (TMP/STX) peroral oder mittels Paromomycin über eine Trinkwasserapplikation zu behandeln. Paromomycin ist eine antimikrobiell wirksame Substanz aus der Gruppe der Aminoglykoside, welche normalerweise nicht oder nur zu einem sehr geringen Anteil systemisch absorbiert wird. Die Ausscheidung findet hauptsächlich über Kot statt. In der Humanmedizin findet Paromomycin Einsatz in der Therapie von Blastocystose, Cryptosporidiose, Amöbenruhr und bei der kutanen Form der Leishmaniose.
Im aktuellen Fall wurde TMP/STX über das Futter verabreicht, was aber zu keinem Behandlungserfolg führte. Aus diesem Grund entschied sich der betreuende Tierarzt Paromomycin in einer Dosierung von 40 mg/kg Körpergewicht für 10 Tage einzusetzen, da es ein registriertes und zugelassenes Produkt für die Anwendung im Schwein gibt. Dieses Produkt ist für die Behandlung von Colienteritis zugelassen.
Aber eine antibiotische Behandlung von Blastocystis alleine wird nicht dauerhaft zu einem Behandlungserfolg führen. Antibiotische Therapie muss immer mit Management-Maßnahmen wie Reinigung und Desinfektion kombiniert werden. Da es im Moment keine Information bezüglich Desinfektionsmittel gibt, welche gegen Blastocystis wirken, wurde angenommen, dass Produkte basierend auf Kresole oder quarternärer Ammoniumverbindungen/Glutaraldehyd wirksam sind. Sollte sich herausstellen, dass andere immunsuppressive infektiöse Erreger eine Rolle spielen, müssen diese auch in der Behandlung mit berücksichtigt werden. Wenn aber Mykotoxine im Verdacht stehen die Erkrankung auszulösen, sollte überlegt werden, ob es eine Möglichkeit gibt gegen diese wirksame Futterzusätze einzusetzen.
Follow up
Nach einigen Monaten verbesserte sich die klinische Situation wesentlich. Paromomycin wurde erfolgreich in drei Durchgängen eingesetzt. In diesen drei Durchgängen konnte kein Durchfall mehr beobachtet werden. Die Mortalitätsrate reduzierte sich auf <1%. Da aber die Behandlung von Absetzferkel mit Paromomycin kostenintensiv wurde, entschied sich der betreuende Tierarzt die metaphylaktische Behandlung zu stoppen. Um aber die Darmgesundheit der Ferkel weiterhin zu unterstützen, wird nun Zinkoxid (2500 ppm) und Aktivkohle über das Futter an Ferkel verabreicht. Nach wie vor ist diese Supplementierung mit Zinkoxid und Aktivkohle ausreichend um Durchfall in Absetzferkel vorzubeugen.
Zusammenfassung und Ausblick
Zusammenfassend sollte Blastocystis sp. in Zukunft auf die Differentialdiagnosenliste bei Durchfallerkrankungen von Ferkeln gesetzt werden, vor allem in Jahren in welchen von einer hohen Mykotoxinbelastung von Mais und Getreide ausgegangen werden kann. Genauso, sollten aber Labore ihr Untersuchungsspektrum bei Schweinen mit profusem Durchfall auf Blastocystis sp. erweitern.






